Die irreversible Elektroporation (IRE), auch bekannt als NanoKnife, ist eine minimalinvasive Ablationstherapie, die bei Prostatakrebs eingesetzt wird. Sie zerstört Prostatatumoren mittels kurzer elektrischer Impulse anstelle von Hitze oder Strahlung und ermöglicht dadurch eine gezielte Zerstörung von Prostatakrebszellen bei weitgehendem Erhalt umliegender Strukturen wie Nerven und Blutgefäßen.
Der Einsatz von IRE hat die therapeutischen Optionen beim Prostatakarzinom erweitert. Sie ermöglicht die Behandlung definierter Tumorareale, ohne die gesamte Prostata zu entfernen, was Auswirkungen auf funktionelle Ergebnisse sowie auf die Möglichkeit weiterer Therapien bei Bedarf hat.
IRE wird in erster Linie als fokale Behandlung bei lokalisiertem Prostatakrebs eingesetzt, kann jedoch – abhängig von Tumorausdehnung und Vorbehandlung – auch in ausgewählten fortgeschrittenen oder inoperablen Fällen angewendet werden.
Diese Seite erläutert die wissenschaftlichen Grundlagen der irreversiblen Elektroporation, beschreibt den Ablauf des NanoKnife-Verfahrens und gibt einen Überblick über veröffentlichte klinische Ergebnisse, Rezidivmuster und Nebenwirkungsdaten bei Prostatakrebs.
NanoKnife
Eine Revolution in der Behandlung con Prostatakrebs
Die irreversible Elektroporation (IRE), auch bekannt als NanoKnife, ist eine minimalinvasive Ablationstherapie, die bei Prostatakrebs eingesetzt wird. Sie zerstört Prostatatumoren mittels kurzer elektrischer Impulse anstelle von Hitze oder Strahlung und ermöglicht dadurch eine gezielte Zerstörung von Prostatakrebszellen bei weitgehendem Erhalt umliegender Strukturen wie Nerven und Blutgefäßen.
Der Einsatz von IRE hat die therapeutischen Optionen beim Prostatakarzinom erweitert. Sie ermöglicht die Behandlung definierter Tumorareale, ohne die gesamte Prostata zu entfernen, was Auswirkungen auf funktionelle Ergebnisse sowie auf die Möglichkeit weiterer Therapien bei Bedarf hat.
IRE wird in erster Linie als fokale Behandlung bei lokalisiertem Prostatakrebs eingesetzt, kann jedoch – abhängig von Tumorausdehnung und Vorbehandlung – auch in ausgewählten fortgeschrittenen oder inoperablen Fällen angewendet werden.
Diese Seite erläutert die wissenschaftlichen Grundlagen der irreversiblen Elektroporation, beschreibt den Ablauf des NanoKnife-Verfahrens und gibt einen Überblick über veröffentlichte klinische Ergebnisse, Rezidivmuster und Nebenwirkungsdaten bei Prostatakrebs.
Rufen Sie uns unter 069 50 50 00 980 jetzt an oder nehmen Sie per Kontaktformular Kontakt auf
Nehmen Sie sich Zeit und informieren Sie sich.
Prostatakrebs schreitet häufig langsam voran. In den meisten Fällen haben Sie ausreichend Zeit, sich über alle Behandlungsmethoden zu informieren. Darüber hinaus verlängert die klassische „radikale“ Therapie (Operation und/oder Strahlentherapie) bei niedrig-aggressiven Prostatakarzinomen nur selten die Lebenserwartung – und bei hochaggressiven Karzinomen tut sie dies laut verfügbarer Statistik bei vielen Männern ebenfalls nicht. Gleiches gilt für die Strahlentherapie.
Gleichzeitig führen die klassischen Behandlungen vor allem zu schweren Nebenwirkungen, jedoch selten zur Heilung: 70–80 % aller Männer leiden nach einer Operation an erektiler Dysfunktion, und etwa 20–50 % der Patienten entwickeln eine Harninkontinenz: Rund 20 % der Männer leiden an schwerer Inkontinenz mit dem Bedarf mehrerer Vorlagen pro Tag, und weitere 30 % an moderater Inkontinenz, bei der eine Vorlage pro Tag ausreichend ist (siehe Tabelle 1).
RT
3.2%
4.4%
9.4%
RT
60.8%
71.9%
93.9%
Darmfunktion
RT
34.0%
31.3%
35.8%
Tabelle 1: Langzeitfolgen der radikalen Prostatektomie (RPE) und der Strahlentherapie (RT) bei Prostatakrebs hinsichtlich Inkontinenz, Impotenz und beeinträchtigter Darmfunktion. Tabelle ins Deutsche übersetzt. Resnik MJ, Koyoma T, Fan K-H, et al. N Engl J Med 2013; 368:436–45.
NanoKnife (IRE): Überblick und klinischer Hintergrund
Das NanoKnife-Gewebeablationsverfahren ist eine neuartige, seit mehr als 10 Jahren eingesetzte Therapie, die die Methode der irreversiblen Elektroporation (IRE) zur Zellzerstörung nutzt. Das umliegende Gewebe wird dabei nicht geschädigt. Mit dieser Methode kann Prostatakrebs erstmals so behandelt werden, dass die Kontinenz erhalten bleibt und nur ein geringes Risiko für Impotenz besteht. Darüber hinaus ist die Wahrscheinlichkeit von Schmerzen oder Narbenbildung beim NanoKnife-Verfahren sehr gering.
Hier bei VITUS sind wir stolz auf die Pionierarbeit, die wir mit dem NanoKnife-Verfahren geleistet haben. Wir gehören weltweit zu den führenden Experten im Einsatz von IRE zur Behandlung von Prostatakrebs.
Durch unsere enge Zusammenarbeit mit dem Erfinder der IRE für medizinische Zwecke, Prof. Boris Rubinsky von der University of Berkeley in den USA, hatten wir die Möglichkeit, IRE in allen Entwicklungsphasen zu studieren und zu verstehen – vom Labor über Tierstudien bis hin zur Anwendung am Menschen. Unsere Physiker und Ärzte zählen daher zu den Pionieren und weltweit führenden Experten im Bereich der Elektroporationsverfahren – sowohl im wissenschaftlich-technischen Bereich als auch in der klinischen Anwendung.
VORTEILE DER
NANOKNIFE-BEHANDLUNG
AUF EINEN BLICK:
- Einmalige Behandlung, abgeschlossen an einem einzigen Tag
- Bisher höchste erreichte Potenzerhaltungsrate*
- Statistisch 0% Inkontinenz**, ***
- Keine chirurgischen Schnitte
- Keine aufwändige Nachsorge notwendig
- Keine höhere Rezidivrate als bei radikalen Verfahren**
- Behandlung auch nach Prostatektomie oder Strahlentherapie möglich
- Sekundäre immunologische Effekte
* Harninkontinenz ist das fehlende oder eingeschränkte Vermögen des Körpers, den Inhalt der Harnblase sicher zu speichern und kontrolliert zu entleeren. Dies führt zu unwillkürlichem Urinverlust. Obwohl es mehrere mögliche Definitionen von Inkontinenz gibt, kommt eine Langzeitstudie zur Inkontinenz nach Prostatektomie** zu dem Schluss, dass eine sinnvolle Definition von Inkontinenz dann vorliegt, wenn ein Patient 12 Monate nach einer Prostataoperation zwei oder mehr Vorlagen pro Tag benötigt.
** Sacco E, Prayer-Galetti T, Pinto F, et al. Harninkontinenz nach radikaler Prostatektomie: Inzidenz nach Definition, Risikofaktoren und zeitlicher Verlauf in einer großen Serie mit Langzeitnachbeobachtung. BJU Int. 2006;97:1234–41.
*** Syan, Raveen, und Victor W. Nitti. „Post-Prostatektomie-Inkontinenz – Erstbewertung.“ Harnfunktionsstörungen bei Prostatakrebs. Springer, Cham, 2016. 15–30. 15-30.
NanoKnife-Technologie bei Prostatakrebs
Das NanoKnife-Verfahren basiert auf ultrakurzen Impulsen, die starke elektrische Felder erzeugen. Die Impulse sind 100 Mikrosekunden lang – also 0,0001 Sekunden. Im Vergleich zu Standardverfahren weist diese neue Technologie einzigartige Eigenschaften auf, die sie ideal für die Behandlung der Prostata machen.
- Das NanoKnife-Verfahren basiert auf ultrakurzen Impulsen, die starke elektrische Felder erzeugen. Die Impulse sind 100 Mikrosekunden lang, also 0,0001 Sekunden. Im Vergleich zu Standardverfahren weist diese Technologie einzigartige Eigenschaften auf, die sie besonders gut für die Behandlung der Prostata geeignet machen.
- Gewebeselektivität: Nur Zellen mit einer Zellmembran, wie Krebszellen, werden zuverlässig zerstört. Alle anderen Strukturen, wie Nerven, Blutgefäße und Bindegewebsstrukturen, bleiben intakt.
- Ultrascharfe Ränder: Mit NanoKnife kann die Grenze zwischen vollständig behandeltem und unbehandeltem Gewebe im Mikrometerbereich gemessen werden. Dies unterscheidet NanoKnife deutlich von anderen Behandlungsmethoden wie Strahlentherapie, wärmebasierten Verfahren und Operation. Bei diesen Methoden ist das zentrale Behandlungsfeld von einem Bereich umgeben, in dem Gewebe unbeabsichtigt geschädigt wird, oft mit einer Ausdehnung von mehreren Zentimetern Durchmesser.
- Programmierter Zelltod: NanoKnife induziert den Zelltod (Apoptose), ohne Strahlenschäden oder Verbrennungen zu verursachen und ohne Narbenbildung. Aktuelle Standardmethoden wie Strahlentherapie (Protonentherapie, Brachytherapie usw.) und wärmebasierte Therapien (HIFU, Mikrowellentherapie usw.) erzeugen ein großes „toxisches“ Areal, da das verbrannte Gewebe für den Körper schädlich ist. Dies kann zu Entzündungen, Schmerzen und nachfolgender Narbenbildung führen, was im Falle eines Rezidivs weitere Behandlungsmöglichkeiten einschränken kann.
- Beliebig oft wiederholbar: Da die IRE-Behandlung keine langfristigen Gewebeschäden verursacht, können andere Behandlungsmethoden (Strahlentherapie, wärmebasierte Verfahren oder Operation) auch nach einer NanoKnife-Behandlung weiterhin durchgeführt werden. Darüber hinaus kann die IRE-Behandlung selbst so oft wie erforderlich wiederholt werden, selbst nach einer bereits erfolgten irreversiblen Elektroporation.
- Schmerzlose und minimalinvasive Therapie: Es kommt zu keiner Gewebeschädigung durch Verbrennung oder Strahlung. Gleichzeitig werden lediglich dünne Nadeln als invasive Instrumente verwendet. Infolgedessen verspüren Patienten während der Behandlung in der Regel nur geringe Beschwerden.
- Schnell und in einer Sitzung: Selbst ausgedehnte Behandlungsareale können häufig in einer einzigen Sitzung unter Vollnarkose behandelt werden.
- Breites Anwendungsspektrum: Die Behandlung kleiner, früh erkannter Prostatatumoren ist die einfachste Anwendung von NanoKnife. NanoKnife kann jedoch auch zur Behandlung inoperabler Karzinome eingesetzt werden, die die Prostatakapsel durchbrochen haben, sowie bei Rezidiven nach Strahlentherapie, radikaler Prostatektomie, hochintensiv fokussiertem Ultraschall (HIFU) oder Brachytherapie.
- Immunsystem: Während der NanoKnife-Behandlung freigesetzte Tumorfragmente unterstützen das Immunsystem des Patienten bei der Bekämpfung weiteren Tumorwachstums.
Präzisionsanforderungen für die NanoKnife-Behandlung
Seit 2007 ist die IRE-Technik in den USA von der FDA zugelassen und in Europa CE-gekennzeichnet. Dies erfolgte, weil entsprechende Studien belegen, dass mit dieser Methode alle Zellen innerhalb des Behandlungsfeldes abgetötet werden können. Um dies zu erreichen und eine erfolgreiche IRE-Behandlung durchzuführen, sind zwei Faktoren entscheidend:
- Erstens:
Die genaue Position des Tumors muss vor der Behandlung bekannt sein. - Zweitens:
Das Behandlungsfeld muss exakt an der richtigen Position platziert werden.
Die erste Voraussetzung wird durch eine multiparametrische MRT-Untersuchung, eine 3D-Biopsie und gegebenenfalls weitere Verfahren erfüllt. Die zweite Voraussetzung wird durch einen minimalinvasiven Eingriff unter Vollnarkose erfüllt. Es werden sterile Nadeln mit variabler Expositionslänge eingeführt. „Expositionslänge“ bezeichnet den Bereich der Nadel, der das Gewebe dem elektrischen Strom aussetzt. Wir verfügen seit 2011 über Erfahrung mit diesem Verfahren und haben weltweit die meisten Prostatabehandlungen durchgeführt. Dies macht uns zu einem der weltweit führenden Experten, während andere Kliniken gerade erst beginnen.
Rufen Sie uns unter 069 50 50 00 980 jetzt an oder nehmen Sie per Kontaktformular Kontakt auf
The NanoKnife Treatment Procedure
Dieser Schritt ist möglicherweise der wichtigste. NanoKnife ist eine fokale, bildgestützte Behandlung, deren Ergebnisse nur so gut sind wie die Planung und Diagnostik, die ihr vorausgehen. Dies liegt daran, dass NanoKnife selbst nicht erkennt, wo sich der Krebs befindet.
Als Patient sollten Sie bei der Diagnostik keine Kompromisse eingehen. Alle Varianten des Ultraschalls (einschließlich Elastographie und kontrastmittelverstärktem Ultraschall) sowie rektale Stanzbiopsien weisen alarmierend niedrige Entdeckungsraten auf. Es ist sehr unwahrscheinlich, dass damit (alle) Tumoren gefunden werden.
Derzeit liefern nur multiparametrische MRT-Untersuchungen, die von spezialisierten radiologischen Instituten durchgeführt werden, eine adäquate bildgebende Diagnostik – gegebenenfalls in Kombination mit PSMA-/Cholin-PET/CT.
Die 3D-Bilder aus der MRT werden durch eine 3D-Sättigungsbiopsie um eine weitere Ebene ergänzt. Wir sind auf beide Verfahren spezialisiert. Beide sind erforderlich, um die diagnostische Genauigkeit zu erreichen, die für eine effektive Durchführung der NanoKnife-Behandlung notwendig ist.
Sobald unsere Ärzte und Physiker anhand der MRT-Querschnittsbilder das Zielgebiet bestimmt und es gegebenenfalls mithilfe von uns entwickelten 3D-Simulationen im Voraus berechnet haben, wird das Zielgebiet gespeichert und am Operationstag auf den OP-Monitor übertragen.
Für die Behandlung der Prostata werden die Nadeln transperineal, also durch den Damm (den Bereich zwischen Genitalien und Anus), eingeführt. Ein endorektaler Ultraschall unterstützt die Platzierung. Erfahrung spielt hierbei eine entscheidende Rolle. Bereits zwei Nadeln stellen hohe Anforderungen an das räumliche Vorstellungsvermögen des Operateurs. Platzierungen mit vielen Nadeln sind äußerst anspruchsvoll. Dies liegt daran, dass die Prostata ein relativ kleines Organ mit komplexer Geometrie ist, das von zahlreichen empfindlichen anatomischen Strukturen umgeben ist. Zudem sind die Positionierungsmöglichkeiten der Nadeln sehr begrenzt. Dieser Prozess kann mitunter mehrere Stunden dauern, wobei uns hier im VITUS Prostatazentrum Computerprogramme helfen, die perfekte Platzierung zu erreichen.
Abbildung 1: Minimalinvasive NanoKnife-Elektrode
Sobald die Nadeln präzise platziert sind, wird ihre Position mittels Ultraschall vermessen und an die NanoKnife-Software sowie weitere externe Software übermittelt. Das zu behandelnde Areal kann am Computer noch durch verschiedene Parameter wie Spannung, Pulsdauer und Anzahl der Pulse angepasst werden. Wenn alle Einstellungen der Geometrie von Prostata und Tumor entsprechen (unter Berücksichtigung eines Sicherheitsabstands um den Tumor), lädt NanoKnife seine Kondensatoren auf.
Zwischen jedem Nadelpaar baut sich eine Potenzialdifferenz auf. Diese beträgt in der Regel 3000 Volt (V). Das bedeutet, dass auf Nadel 1 +1500 V und auf Nadel 2 -1500 V anliegen. Der Patient verbleibt bei 0 V. Diese Spannungen mögen lebensbedrohlich erscheinen, doch ihre Wirkungsdauer liegt im Bereich von Millionstelsekunden. Dadurch ist das Verfahren sicher, und Nebenwirkungen wie Verbrennungen werden vermieden. Weitere Informationen zur Technologie und zur zugrunde liegenden Theorie finden Sie hier im Abschnitt zur Theorie der IRE.
Die Anzahl der Nadeln kann variieren und hängt maßgeblich vom zu behandelnden Areal ab. Der Computer des NanoKnife-Systems übernimmt entsprechend den zuvor festgelegten Einstellungen die Steuerung der Nadeln. Die eigentliche Behandlung dauert in der Regel nur Sekunden, maximal wenige Minuten.
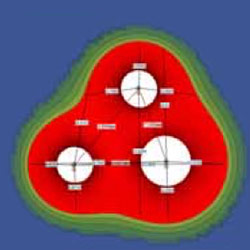
Abbildung 2: Präzise Planung der IRE-Behandlung
Unmittelbar nach dem Herausziehen der Nadeln schließen sich die Einstichstellen wieder. Die meisten Patienten verspüren keine Schmerzen. Einige empfinden jedoch den vor der Behandlung eingesetzten Blasenkatheter als unangenehm. Er kann nach 10 bis 14 Tagen entfernt werden. Auch mehrere Wochen später können noch geringe Mengen Blut im Urin oder in der Samenflüssigkeit zu finden sein. Das liegt daran, dass der Körper bis zu sechs Monate braucht, um das durch die NanoKnife-Ablation zerstörte Gewebe aus dem Körper zu entfernen.
Wie IRE im Vergleich zur radikalen Prostatektomie hinsichtlich klinischer Ergebnisse abschneidet
Während bisher mehr als 2.000 Männer mit Prostatakrebs in der VITUS Privatklinik erfolgreich behandelt wurden (Stand Januar 2026), basieren die veröffentlichten Ergebnisdaten auf 471 IRE-Behandlungen mit einer maximalen Beobachtungsdauer von 7 Jahren².
Tabelle 2 zeigt, dass die Mehrheit der behandelten Patienten gemäß der D’Amico-Klassifikation ein Hochrisiko-Prostatakarzinom aufwies.
Tabelle 2
Die meisten Karzinome wurden als Stadium T2a bis T2c klassifiziert, was bedeutet, dass sie auf die Prostata begrenzt waren und die Prostatakapsel makroskopisch noch nicht durchbrochen hatten („organbegrenzte Erkrankung“). Allerdings wurden auch 84 Patienten mit T3- und T4-Karzinomen behandelt, also Tumoren, die sich bereits über die Prostatakapsel hinaus ausgedehnt hatten („nicht organbegrenzte Erkrankung“).
Unsere Behandlungsergebnisse zeigen, dass IRE nicht nur für die Behandlung früher, lokalisierter Prostatakarzinome geeignet ist, sondern auch für die effektive Behandlung fortgeschrittener Karzinome.
T4 N0 M1 /
T4 N1 M1
Tabelle 3
Während der Beobachtungszeit von bis zu 70 Monaten traten 4 Rezidive bei Patienten mit niedriggradigen Gleason-6-Karzinomen, 15 Rezidive bei Patienten mit intermediären Gleason-7-Karzinomen und 22 Rezidive bei Patienten mit hochgradigen Gleason-8–10-Karzinomen auf.
Verglichen mit den Rezidivraten nach radikaler Prostatektomie (RPE), wie sie in den Han-Tabellen der Johns Hopkins University berichtet werden, sind die Rezidivraten nach IRE vergleichbar mit denen nach RPE.
Rezidivraten nach IRE-Behandlung
Wie „Rezidiv“ beim Prostatakrebs interpretiert wird
Nach radikaler Entfernung der Prostata würde man erwarten, dass der Krebs vollständig aus dem Körper entfernt ist. Dies ist jedoch nicht immer der Fall und liefert einen wichtigen Kontext für die Interpretation von Rezidivraten nach fokalen Therapien wie IRE.
Ein genauerer Blick in die Han-Tabellen zeigt, dass die Rezidivraten nach radikaler Prostatektomie erheblich bleiben, selbst wenn der Tumor vollständig zusammen mit der Prostata entfernt wurde (Kategorie „organbegrenzte Erkrankung“).
Woher stammen diese Rezidive?
Sie entstehen aus einzelnen Tumorzellen, die entlang von Bindegewebsstrukturen, Lymphbahnen und Blutgefäßen aus der Prostata ausgewandert sind und sich im die Prostata umgebenden Bindegewebe eingenistet haben. Tumorzellen können auch im Blutkreislauf zirkulieren und mittels Liquid-Biopsy-Verfahren nachgewiesen werden.
Dies geschieht, weil die Prostatakapsel für Zellen durchlässig ist, da sie aus verdichtetem Bindegewebe und nicht aus einer festen Barriere besteht. Dies lässt sich mit dem Bild eines Waldrandes veranschaulichen: Aus der Ferne wirkt er geschlossen, bei näherer Betrachtung besteht er jedoch überwiegend aus offenen Zwischenräumen mit einzelnen strukturellen Elementen.
Entsprechend treten viele Rezidive nach Prostatektomie im Bindegewebe auf, das zuvor die Prostata umgeben hat und auch nach ihrer Entfernung die Prostataregion weiterhin umgibt.
Streng genommen stellen alle lokalen Prostatakrebstherapien eine Tumormassenreduktion dar, also die Zerstörung oder Entfernung von Tumorgewebe innerhalb der Prostata. Tumorzellen außerhalb der Prostata können im Körper verbleiben und im Erfolgsfall vom körpereigenen Immunsystem kontrolliert werden.
Vor diesem Hintergrund ist es nicht überraschend, dass die Rezidivraten nach IRE-Behandlung mit denen nach radikaler Prostatektomie und Strahlentherapie vergleichbar sind.
Beobachtete Rezidivraten nach IRE-Behandlung
Tabelle 4
Tabelle 4 zeigt die Anzahl rezidivierender Prostatakarzinome, die über einen maximalen Nachbeobachtungszeitraum von 70 Monaten in den verschiedenen Gleason-Score-Gruppen unter 471 an der VITUS Privatklinik durchgeführten IRE-Behandlungen beobachtet wurden.
Wie erwartet traten die meisten Rezidive bei Patienten mit hochgradigem Prostatakrebs (Gleason 8–10) auf, weniger in der Gleason-7-Gruppe und die wenigsten in der Gleason-6-Gruppe.
Kaplan–Meier-Analyse und Vergleich mit radikaler Prostatektomie
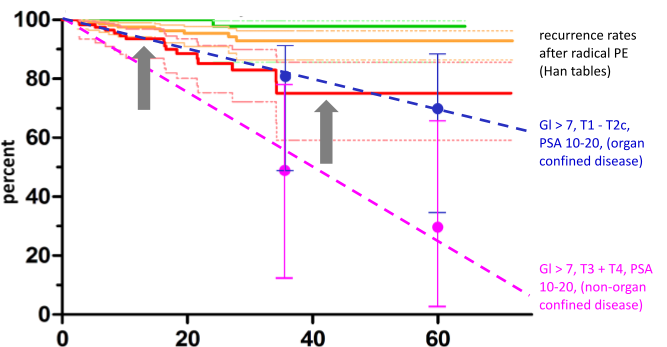
Die Grafik in Abbildung 1 zeigt die Kaplan–Meier-Kurven der 471 ausgewerteten IRE-Behandlungen. Diese Kurven veranschaulichen die Anzahl der Patienten, die im zeitlichen Verlauf nach IRE-Behandlung ein Prostatakrebsrezidiv entwickelten, stratifiziert nach Tumoraggressivität (Gleason 6, Gleason 7 und Gleason 8–10). Der maximale Beobachtungszeitraum betrug 70 Monate.
Von besonderem Interesse ist der Vergleich zwischen den Rezidivraten bei aggressiven Prostatakarzinomen (rote Kurve) und den Rezidivraten nach radikaler Prostatektomie (RPE), wie sie in den Han-Tabellen der Johns Hopkins University, USA (blaue und rosafarbene gestrichelte Linien), berichtet werden.
Dieser Vergleich wurde anhand von Daten von Patienten mit vergleichbarem Tumorstadium und Gleason-Score durchgeführt.
Die Rezidivraten nach IRE-Behandlung bei aggressiven Karzinomen liegen innerhalb des „Korridors“ der nach radikaler Prostatektomie beobachteten Rezidivraten und sind somit vergleichbar.
Lokalisation der Rezidive nach IRE-Behandlung
Die Lokalisation der Rezidive liefert zusätzliche Erkenntnisse.
Insgesamt traten nur 8 der 41 beobachteten Rezidive innerhalb des IRE-Ablationsfeldes auf, und 15 traten unmittelbar angrenzend an das behandelte Areal auf. Diese Fälle sind auf überlebende Tumorzellen innerhalb oder unmittelbar außerhalb des abladierten Tumorfokus zurückzuführen.
Allerdings traten 16 der 41 berichteten „Rezidive“ in Bereichen der Prostata auf, die vor der Behandlung als tumorfrei beurteilt worden waren und daher nicht behandelt wurden.
Diese Fälle stellen kleine, zuvor nicht erkannte Karzinomherde dar, am häufigsten bei Patienten, die eine umfassende diagnostische Abklärung wie 3D-Mapping-Biopsie (3DMB), hochwertige endorektale MRT und/oder PSMA-PET/CT mit Gallium-68 abgelehnt hatten.
Streng genommen handelt es sich hierbei nicht um echte Rezidive, sondern um zusätzliche Tumorherde, die vor der Behandlung nicht identifiziert wurden.
Wenn diese „Pseudo-Rezidive“ aus der Statistik entfernt und die Kaplan–Meier-Kurven auf Grundlage der tatsächlichen Rezidive neu berechnet werden, zeigen sich längere rezidivfreie Überlebenszeiten. Dieser Effekt ist in Grafik X dargestellt, in der sich die Kaplan–Meier-Kurve für das rezidivfreie Überleben nach oben verschiebt (graue Pfeile).
Klinisches Beispiel einer fokalen IRE-Behandlung
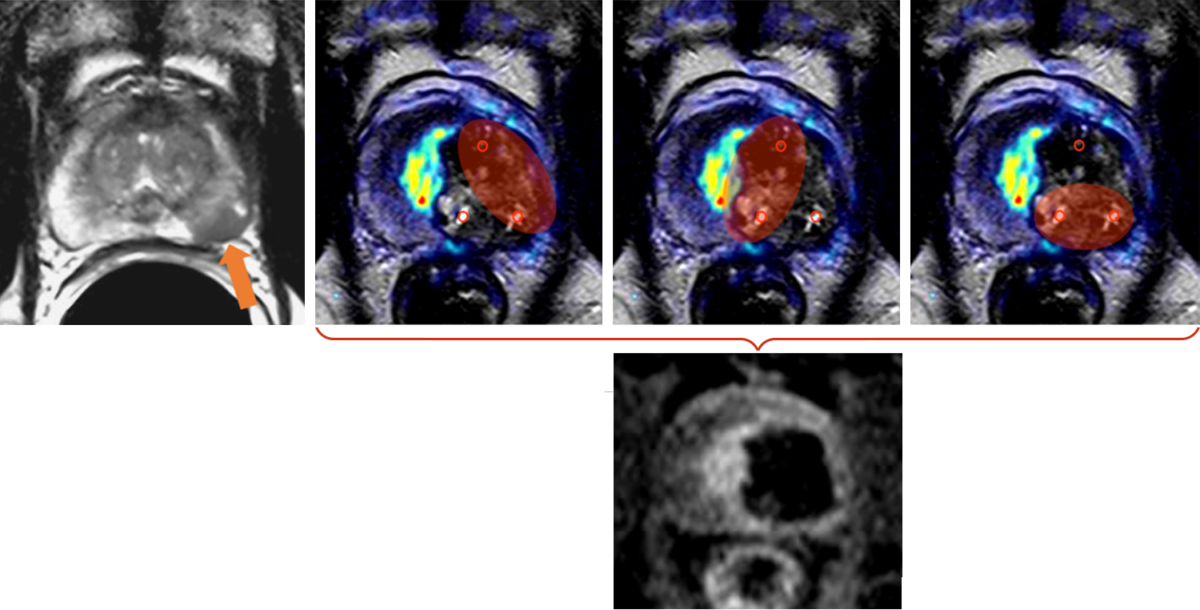
Pro Elektrodenpaar wurde eine Ablationszone erzeugt (rote Ellipsen). Nach Kontrastmittelgabe ist die Ablationszone als avaskuläres Areal ohne Blutversorgung klar erkennbar. Der PSA-Wert sank von 5,2 ng/ml vor der Behandlung auf 2,3 ng/ml nach IRE und nicht auf null, da der rechte Prostatlappen erhalten blieb. Dies ist typisch für fokale Therapien bei Prostatakrebs.
Abbildung 2 zeigt die Behandlung eines Prostatakarzinoms (Stadium T2b, N0, M0, Gleason 7b) in der linken dorsalen Außenzone (Pfeil; radiologische Orientierung, Ansicht von unten, rechts und links vertauscht) bei einem 53-jährigen Mann.
Die Behandlung wurde mit 3 Elektroden durchgeführt, deren Positionen am Tag nach der Behandlung sichtbar sind (kleine rote Kreise). Pro Elektrodenpaar wurde eine Ablationszone erzeugt (rote Ellipsen).
Im Bild nach Kontrastmittelgabe ist die Ablationszone als avaskuläres Areal ohne Blutversorgung deutlich erkennbar.
Der PSA-Wert sank von 5,2 ng/ml vor der Behandlung auf 2,3 ng/ml nach IRE und nicht auf null, da der rechte Prostatlappen erhalten blieb. Dies ist typisch für fokale Therapien.
Sicherheitsprofil der IRE bei Prostatakrebs
Tabelle 5 unten zeigt Nebenwirkungen, die bei der Behandlung von 471 Prostatakrebspatienten in der VITUS Privatklinik auftraten.
Zunächst ist hervorzuheben, dass keine lebensbedrohlichen Nebenwirkungen und keine behandlungsbedingten Todesfälle auftraten. Dies spiegelt den minimalinvasiven Charakter des Verfahrens wider.
Leichte Nebenwirkungen traten bei etwa einem Fünftel der mit IRE behandelten Patienten auf (grüne Felder). Dazu gehörten vorübergehende Schwierigkeiten beim Wasserlassen (Harnverhalt), die das erneute Einlegen eines Blasenkatheters nach Entfernung des ersten Katheters erforderlich machten.
In solchen Fällen blieb der Katheter in der Regel weitere 10–14 Tage liegen. Leichte Beschwerden oder Schmerzen beim Wasserlassen (Dysurie) traten bei etwa 7% der Patienten auf, und eine leichte Hämaturie (Blut im Urin) bei etwa 4%.
Mäßig schwere unerwünschte Ereignisse traten nur bei 2,5% der mit IRE behandelten Patienten auf (gelbe Felder). Dabei handelte es sich um katheterassoziierte Harnwegsinfektionen, die mit Antibiotika behandelt wurden.
Medizinisch relevante, jedoch nicht lebensbedrohliche unerwünschte Ereignisse traten bei 1,3% der Patienten auf (rosa Felder).
Dazu gehörten anhaltende Miktionsprobleme durch nekrotisches Tumorgewebe innerhalb der Prostata, die eine transurethrale Resektion (TURP) erforderlich machten; eine rektoprostatale Fistel (Fehlverbindung), die spontan ohne Operation ausheilte; sowie eine durch einen Katheter verursachte Blasenperforation, die ebenfalls spontan verheilte.
Nur klinische oder diagnostische Überwachung – keine Behandlung erforderlich
(19.5%)
(9.0%)
(6.7%)
(3.8%)
Minimale, lokale oder nicht-invasive Behandlung erforderlich; Einschränkung altersentsprechender Alltagsaktivitäten
(2.5%)
(2.5%)
(0.8%)
(0.8%)
(0.2%)
(0.2%)
Dringende medizinische Maßnahmen erforderlich
Harnkontinenz nach IRE-Behandlung
In der VITUS Privatklinik haben wir bei über 2.000 Patienten nach IRE-Behandlung eine Inkontinenzrate von 0% beobachtet. Im Vergleich dazu ist Inkontinenz bei etwa 50% der Männer nach radikaler Prostatektomie, mit oder ohne da-Vinci-Roboterunterstützung, eine häufige und schwerwiegende Nebenwirkung.
Inkontinenz ist bei der chirurgischen Entfernung der Prostata schwer zu vermeiden, da der Blasenschließmuskel, auch unterer Harnröhrenschließmuskel (LUS) genannt, direkt unterhalb der Prostata liegt und bis in die Prostatenspitze (Apex) hineinreicht.
Wird die Prostata entfernt, wird auch ein Teil des Schließmuskels entfernt. Zusätzliche Schäden am LUS entstehen, wenn der Blasenboden nach unten vernäht und nach Entfernung der Prostata mit dem Schließmuskel verbunden wird, um den Harnfluss wiederherzustellen.
Bei mehr als 2.000 bisher mit IRE behandelten Patienten ist keine dauerhafte Inkontinenz aufgetreten. Dies lässt sich leicht feststellen, da behandelte Patienten selbst geringfügigen unwillkürlichen Urinverlust sofort melden. Dennoch erleben unmittelbar nach der IRE-Behandlung ein kleiner Prozentsatz der Patienten eine vorübergehende Inkontinenz aufgrund zweier Mechanismen:
- Dehnung des Schließmuskels durch den Katheter, der 10 bis 14 Tage in der Harnblase verbleibt.
- Dranginkontinenz infolge einer Reizung der Prostata nach Tumorzerstörung, ähnlich wie bei einer Prostatitis. Dies äußert sich dadurch, dass betroffene Männer bei voller Blase plötzlich starken Harndrang verspüren und auf dem Weg zur Toilette Urin verlieren können.
Diese Formen der Inkontinenz sind vorübergehend und klingen in der Regel innerhalb weniger Tage bis maximal drei Monate ab. Sie stehen nicht im Zusammenhang mit der irreversiblen Zerstörung des Schließmuskels, wie sie nach einer Operation auftritt.
Tabelle 6 zeigt unsere veröffentlichten Daten zur Harninkontinenz.
Erektile Funktion nach IRE-Behandlung
Nach IRE-Behandlung bei Prostatakrebs liegen die Impotenzraten zwischen 0 und maximal 10%.
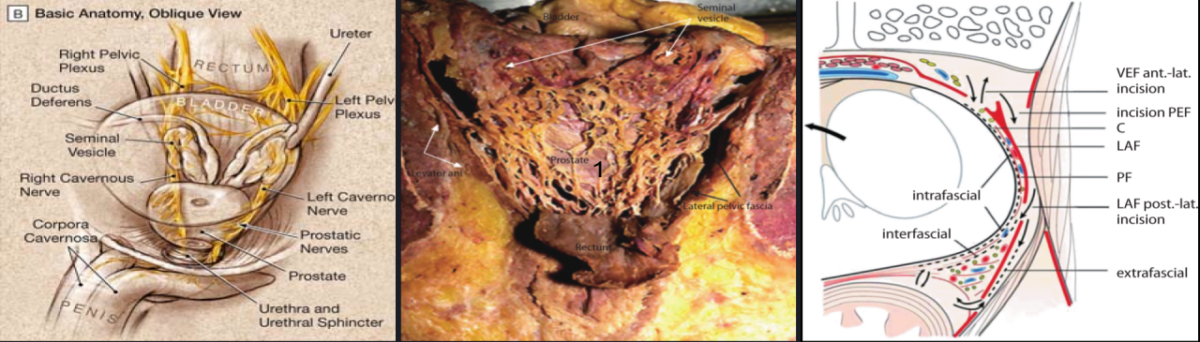
Das neurovaskuläre Bündel (NVB), ein Netzwerk aus Nerven und Blutgefäßen, ist für die Erektionsfähigkeit des Penis verantwortlich. Es liegt überwiegend innerhalb und unmittelbar angrenzend an die Prostatakapsel (siehe Abbildung 2) und kann daher weder bei radikaler Prostatektomie noch bei Strahlentherapie erhalten werden.
Daher sind die Impotenzraten nach konventionellen Prostatakrebsbehandlungen sehr hoch und liegen selbst nach sogenannter „nervenschonender Prostatektomie“ zwischen 60–90%. Das Ergebnis ist der Verlust der erektilen Funktion, also Impotenz.
Klinische Beispiele: IRE bei fortgeschrittenem und inoperablem Prostatakrebs
IRE-Behandlung bei inoperablem Prostatakrebs mit lokaler Organinfiltration
Die Behandlung wurde mit fünf Elektroden durchgeführt, deren Positionen am Tag nach der Behandlung sichtbar sind (kleine schwarze Kreise). Pro Elektrodenpaar wurde eine Ablationszone erzeugt (rote Ellipsen), sodass insgesamt neun einzelne Ablationszonen entstanden. Im Bild nach Kontrastmittelgabe ist die gesamte Ablationszone deutlich als avaskuläres Areal ohne Blutversorgung erkennbar.
Das Prostatagewebe wurde vollständig zerstört, während die Prostatakapsel erhalten blieb, da sie größtenteils aus Bindegewebe besteht, das durch IRE nicht zerstört wird. Der PSA-Wert sank auf 0 ng/ml, vergleichbar mit den Werten nach einer Prostatektomie.
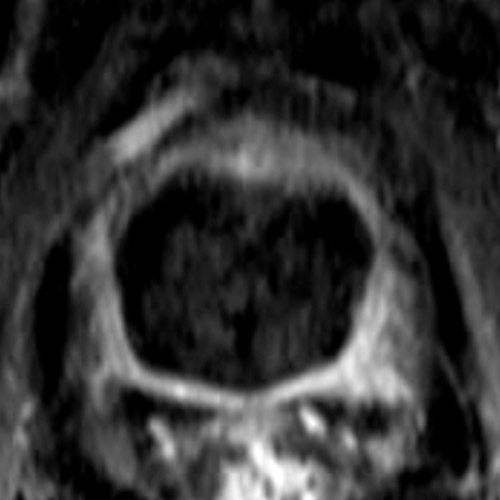
PSA 11 ng/ml
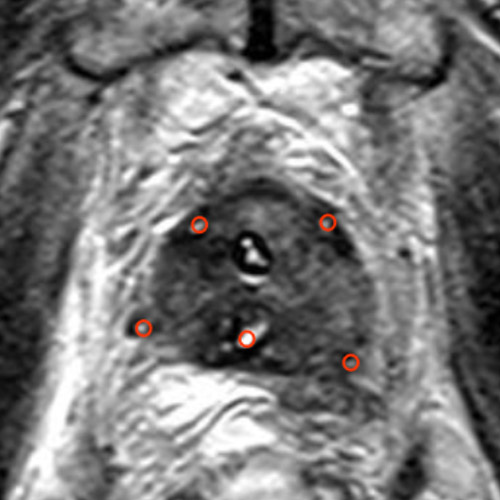
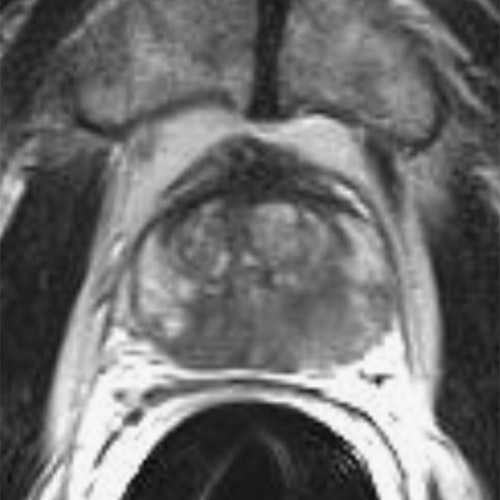
PSA 0,0 ng/ml
Die Bilder zeigen die Behandlung eines Prostatakarzinoms Stadium T2c, N0, M0, Gleason-Score 8, bei einem 63-jährigen Mann. Das Karzinom hatte sich über beide Prostatlappen ausgebreitet. In diesem Fall war eine fokale Therapie unter Erhalt wesentlicher Anteile gesunden Prostatagewebes nicht mehr möglich.
Komplette Prostataablation mittels irreversibler Elektroporation (IRE)
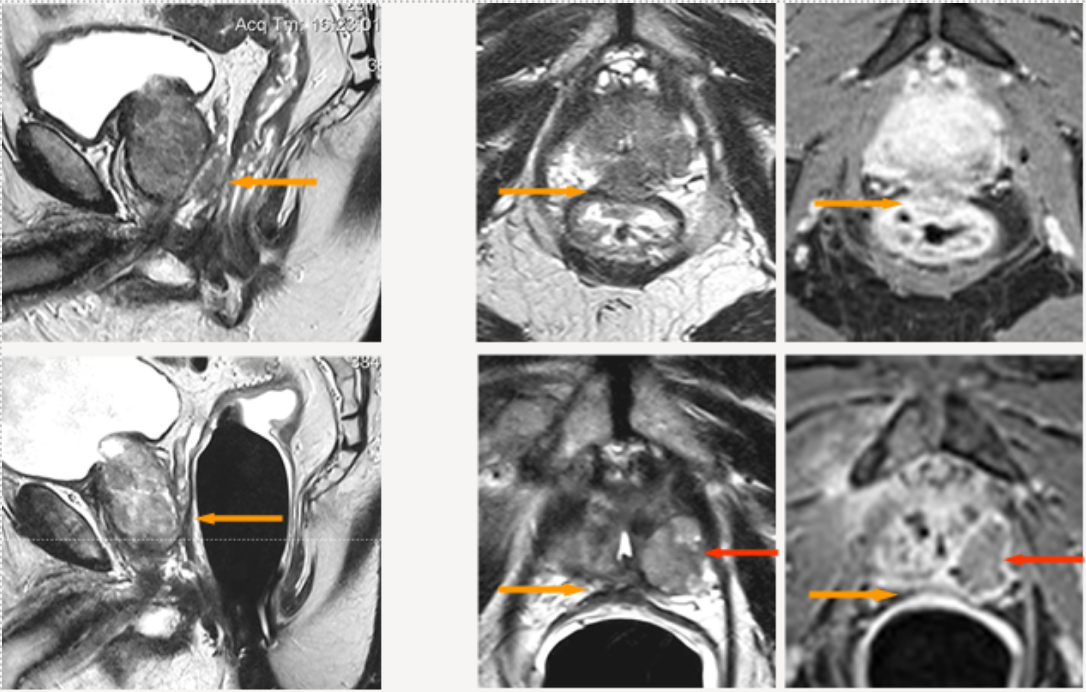
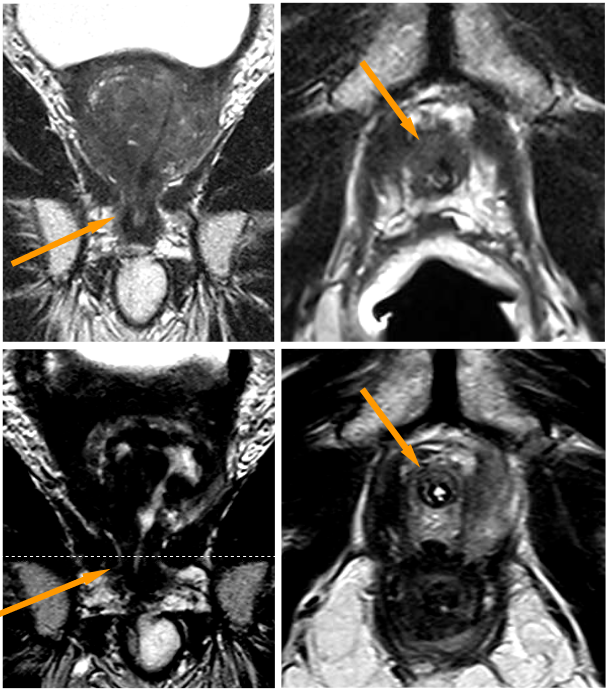
Abbildung 3 zeigt die Behandlung eines Prostatakarzinoms Stadium T4, N0, M0, Gleason-Score 8, bei einem 79-jährigen Mann mit Infiltration des Rektums (Rektumbereich durch gelbe Pfeile gekennzeichnet). Eine radikale Prostatektomie hätte zusätzlich die Entfernung des Rektums sowie die Anlage eines dauerhaften künstlichen Darmausgangs (Anus praeter) erfordert, wodurch der Stuhl in einen externen Beutel abgeleitet worden wäre.
Die Rektuminfiltration ist in den MRT-Bildern in der oberen Reihe von Abbildung 3 dargestellt:
- Links: sagittale Aufnahme
- Mitte: axiale T2-gewichtete Aufnahme
- Rechts: axiale Aufnahme nach Kontrastmittelgabe
Die untere Reihe zeigt den Befund neun Monate nach der IRE-Behandlung. Die Rektumwand erscheint normal, ohne Verletzung und ohne Fistel (abnorme Verbindung) zur Prostata.
Inoperabler Prostatakrebs und fortgeschrittene Behandlungsoptionen
In der VITUS Privatklinik betonen wir, wie wichtig es ist, sich Zeit zu nehmen und die für Ihren individuellen Fall am besten geeignete Behandlungsoption zu finden, beginnend mit sorgfältiger Planung und präziser Diagnostik. In manchen Fällen erfassen Standarddiagnostiken das volle Ausmaß inoperabler Prostatakarzinome vor Therapieentscheidungen nicht vollständig.
Wenn das tatsächliche Tumorausmaß erst intraoperativ erkannt wird, muss die Operation möglicherweise abgebrochen werden oder der Krebs wird unvollständig entfernt, was mitunter die Entfernung von Blase und Rektum sowie die Anlage dauerhafter künstlicher Ausgänge erforderlich macht. In solchen Situationen sind Patienten häufig auf weiterführende Behandlungsansätze angewiesen.
In der VITUS Privatklinik haben wir Dutzende Patienten mit inoperablen oder fortgeschrittenen Prostatakarzinomen erfolgreich behandelt und dabei funktionelle Ergebnisse erhalten. Durch geeignete Bildgebung, Biopsietechniken und sorgfältige Therapieplanung können viele dieser schwerwiegenden chirurgischen Folgen vermieden werden.
Wenn Sie von fortgeschrittenem Prostatakrebs betroffen sind oder Ihnen mitgeteilt wurde, dass die Standard-Operationsmöglichkeiten eingeschränkt sind, können Sie eine individuelle medizinische Bewertung anfordern, um besser zu verstehen, ob unsere minimalinvasiven Behandlungsoptionen für Ihren Fall geeignet sein könnten.
